1º BACHILLERATO METALES NO FERROSOS 1 INTRODUCCIÓN LOS
1 FILOSOFÍA DE 1º DE BACHILLERATO COMENTARIO DE TEXTO1 RECURSOS EDUCATIVOS BACHILLERATO PIZARRA DIGITALECONOMÍA Y ORGANIZACIÓN
10 LENGUA CASTELLANA Y LITERATURA 2º DE BACHILLERATO TEMA
13 LENGUA CASTELLANA Y LITERATURA 2º DE BACHILLERATO
13 Lengua Castellana y Literatura 2º de Bachillerato Tema
16 PARA 2º DE BACHILLERATO PROFESOR JOSÉ TORRES HURTADO
TECNOLOGÍA INDUSTRIAL METALES NO FERROSOS CURSO 2015-16
1º BACHILLERATO

METALES NO FERROSOS:
1.- INTRODUCCIÓN - Los metales no ferrosos y su comienzo
2.-CLASIFICACIÓN DE LOS METALES. – Propiedades y clasificación.
3.-METALES NO FERROSOS PESADOS.
4.-METALES NO FERROSOS LIGEROS.
5.-METALES NO FERROSOS ULTRALIGEROS.
6.- IMPACTO MEDIOAMBIENTAL.
7.-PRESENTACIONES COMERCIALES.


1.-INTRODUCCIÓN:
1.1.Los metales no ferrosos y su comienzo de extracción.
Los metales no ferrosos son aquellos en cuya composición no se encuentra el hierro. Los más importantes son siete: cobre, zinc, plomo, estaño, aluminio, níquel y magnesio. Hay otros elementos que con frecuencia se fusionan con ellos para preparar aleaciones de importancia comercial. También hay alrededor de 15 metales menos importantes que tienen usos específicos en la industria. Los metales no ferrosos se clasifican en pesados, ligeros y ultraligeros.
La segunda época de la cultura humana empieza cuando el hombre aprendió que ciertas clases de minerales se les puede calentar y dar formas, es decir, se les puede forjar o darles forma por medio de un molde, que al enfriar retiene la forma deseada. Además aumenta su dureza y se hace más duradero, e incluso podía conseguirse un filo. Esta época se conoce con el nombre de la Edad de Bronce, aunque anteriormente ya se hubiese utilizado el cobre más o menos puro.
El primer hecho sobresaliente de esa época es el conocimiento de la transformación radical de las propiedades físicas de ciertas sustancias por el calor. El primer forjador descubrió que el cobre natural, sustancia rojiza intratable y relativamente dura, se hacía maleable y plástica al aplicarle calor. El arte del forjador era tan complicado que requería un prolongado aprendizaje, y sus productos eran muy importantes para el desenvolvimiento de la vida.
Para producir el cobre era necesario, calentar con carbón vegetal y fundir la mena a grandes temperaturas, insuflando una corriente continua de aire, soplando mediante pipas. El forjador convertía la masa de cobre en las medidas del comprador.
2.Características generales y clasificación.
Características generales:
Son todos los metales que no contienen en su composición al hierro.
No se utiliza tanto como los metales férreos pero son muy útiles por:
Su bajo peso específico.
Su resistencia a la oxidación.
Su facilidad para manipularlos y mecanizarlos.Tienen numerosas aplicaciones a partir de
sus aleaciones:
De la aleación del cobre, níquel y aluminio obtenemos las monedas.
Del wolframio obtenemos los filamentos de las bombillas.
De la aleación del estaño y el plomo, tenemos el material de soldadura de los componentes electrónicos Del cromo, níquel y cinc obtenemos recubrimientos.
Son caros comparados con los metales ferrosos pero con el aumento de su demanda y las innovaciones técnicas se ha conseguido abatir sus costos, por lo que su competitividad ha crecido notablemente.
Clasificación:
Podemos dividir a los materiales no ferrosos en tres grandes grupos:
-Metales no ferrosos pesados: Son aquellos cuya densidad es igual o mayor a 5 gr/cm3. Son el cobre, el estaño, el plomo, el cinc, el níquel, el cromo y el cobalto.
-Metales no ferrosos ligeros: Tienen una densidad comprendida entre 2 y 5 gr/cm3. Son el aluminio y el titanio.
-Metales no ferrosos ultraligeros: Su densidad es menor a 5 gr/cm3. Son el berilio y el magnesio.
3.-METALES NO FERROSOS PESADOS:
Su densidad es igual o mayor de 5kg/dm cúbico. Tales como: estaño, cobre, zinc, plomo, níquel, Wolframio y Cobalto.
Los más importantes o principales son: estaño y cobre:
3.1.-ESTAÑO:
Estado Natural: Pocas veces se encuentra en estado nativo. Se obtiene principalmente de la casiterita (SnO2), que contiene 79% de estaño.

Características: su densidad es de 7,28 kg/dm³, su punto de fusión alcanza los 231ºC
-Tiene una resistencia a la tracción de 5 kg/mm². En estado puro tiene un color muy brillante, pero a temperatura ambiente se oxida.-A temperatura ambiente es también muy maleable, sin embargo en caliente es frágil y quebradizo.--Por debajo de -18ºC se empieza a descomponer convirtiéndose en un polvo gris, este proceso es conocido como peste del estaño.
Aleaciones y aplicaciones: las aleaciones más importantes son el bronce (cobre + estaño) y las soldaduras blandas (plomo + estaño con proporciones de este entre el 25% y el 90%). Las aplicaciones más importantes son la fabricación de hojalata y proteger al acero contra la oxidación.
3.2-COBRE:
Los minerales de cobre más utilizados en la actualidad se encuentran en forma de cobre nativo, sulfuros (calcopirita y calcosina) y óxidos (malaquita y cuprita) (imagen inferior).
Características:
-Es muy dúctil (se obtienen hilos muy finos) y maleables (pueden formarse láminas hasta de 0,02 mm de espesor)
-Posee una alta conductividad eléctrica y térmica.
Dos métodos de obtención del cobre: por vía seca y por vía húmeda.
• Proceso de obtención del cobre por vía seca: Se utiliza cuando el contenido de cobre supera el 10 %. En caso contrario, será necesario un enriquecimiento o concentración. Es el proceso más empleado y es igualmente usado para el estaño.
Las fases del proceso pueden verse en la imagen inferior.
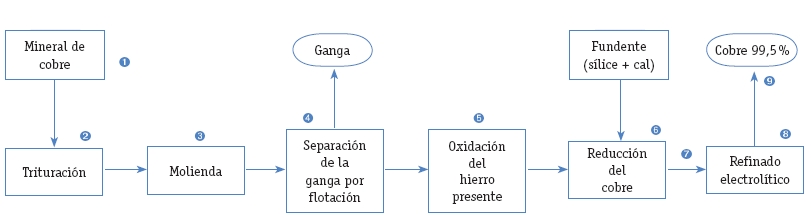
a) El mineral de cobre (1) se introduce en la trituradora (2).Luego se pasa por un molino de bolas (3) con objeto de pulverizarlo. Este molino consta de un cilindro con agujeros muy finos, por donde saldrá el mineral pulverizado.
b) Para separar la mena de la ganga, se introduce el mineral en polvo en un depósito lleno de agua (4) y se agita. El mineral, más pesado, se irá al fondo, mientras que la ganga flotará y se sacará por arriba. (Proceso de decantación).
c) El mineral concentrado se llevará a un horno (5), donde se oxidará parcialmente. El objetivo es oxidar el hierro, pero no el cobre. Se calienta lentamente la mena(mineral sin limpiar) porque pasa por un mecanismo. De esta manera se consigue separar el hierro del cobre.
d) A continuación se introduce todo en un horno (6), donde se funde. Se le añade sílice y cal para que reaccione con el azufre y el óxido de hierro y forme la escoria. El cobre aquí obtenido, tiene una pureza aproximada del 40 % y recibe el nombre de cobre bruto. Si se quiere obtener un cobre de pureza superior al 99,9 % (9), es necesario un refinado electrolítico en la cuba (8).
Aleaciones:
Dos
de las aleaciones de cobre más conocidas, son el latón
(donde se mezcla con zinc) y el bronce (donde se mezcla con
estaño).
La industria del cobre continúa
desarrollando aleaciones innovadoras que aprovechan la versatilidad
del cobre para nuevas aplicaciones. Hoy en día, el cobre se
mezcla con una gran variedad de metales, incluidos el aluminio, el
níquel, el silicio, el manganeso, la plata y el telurio.
Constantemente se están desarrollando nuevas aleaciones que
satisfacen las crecientes necesidades que se
dan
en el campo de la electrónica, los superconductores, el
transporte y la sanidad.
4.-Metales no ferrosos ligeros
4.1.Aluminio:
Estado Natural:
No se presenta nunca en estado nativo. Se extrae exclusivamente de la bauxita.
Propiedades:
Es un metal dúctil y maleable. No lo ataca el aire porque se recubre de una ligera capa de óxido que lo protege. Tiene muy buena conductividad tanto eléctrica como térmica.
Aplicaciones:
Se emplea por sus buenas propiedades eléctricas en la fabricación de alambres destinadas a construcción eléctrica. El aluminio también se emplea en forma de plancha, en el recubrimiento de techos.
Método de extracción:
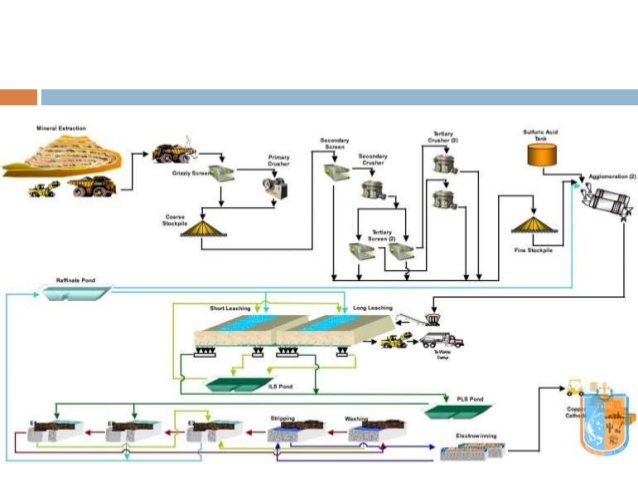
El método Bayer es el más empleado por resultar el más económico. Consta de dos fases:
Obtención de la aluminia:
La bauxita de tritura y se muele hasta que queda pulverizada, se almacena hasta que se vaya a consumir. En un mezclador se introduce la bauxita en polvo, sosa cáustica, cal y agua caliente. La bauxita se disuelve en la sosa. En el decantador se separan los residuos. En el intercambiador de calor se enfría la disolución y se le añade agua. En el recipiente se precipita la aluminia y un filtro permite separar la aluminia de la sosa y esta se calienta a 1200 grados centígrados para eliminar la humedad y posteriormente se enfría a temperatura ambiente.
Obtención del aluminio:
Se disuelve la alúmina en criolita fundida que protege al baño la oxidación, y se le somete a un proceso de electrólisis que descompone el material en aluminio y oxígeno.
La obtención del aluminio a partir de la bauxita, precisa de gran cantidad de energía, por lo que es importante su reciclado.
4.2.Titanio:
Estado natural:
Nunca se encuentra en estado puro aunque es muy abundante en la corteza terrestre. Existe como óxido en los minerales Ilmenita, Rutilo y Esfena.
Propiedades:
Ligero, altamente resistente a la corrosión, dúctil y fuerte. Más rígido y resistente que el acero. Puede ser fundido, estampado y soldado.
Aplicaciones:
Debido a su resistencia y a su peso ligero, el titanio se usa en aleaciones metálicas y como sustituto del aluminio. Aleado con aluminio y vanadio, se utiliza en los aviones. Su uso también es apreciado en la estructura de los misiles y las sondas espaciales.
La relativa inercia del titanio le hace eficaz como sustituto de los huesos y cartílagos en cirugía, así como para las tuberías y tanques que se utilizan en la elaboración de los alimentos.
Proceso de obtención:
Es un proceso complejo que encarece extraordinariamente el producto final.
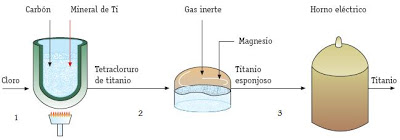
Se emplea casi exclusivamente el método Kroll, que consta de tres fases:
1.Cloración:
Se calienta el mineral de titanio al rojo vivo. Se le añade carbón y se hace circular cloro a través de toda la masa. Se obtiene tetracloruro de titanio.
2.Transformación:
El compuesto se introduce en un horno a 800 grados centígrados. Se introduce un gas inerte, helio o argón, y magnesio. Se forma titanio esponjoso.
3.Obtención:
El titanio esponjoso se introduce en un horno eléctrico y se le añaden fundentes: el resultado es titanio puro.
5.-Metales no ferrosos ultraligeros.
Los metales no ferrosos ultraligeros son uno de los tres grupos en los que se dividen los metales no ferrosos.
Se caracterizan por su densidad, que es menor a 2 kg/dm3. En este grupo destacan el Magnesio y el Berilio.
5.1.-Magnesio:

Características:
Es un metal de color blanco plateado brillante, ligero, blando, maleable y poco dúctil. Su símbolo es Mg y su número atómico 12. Es el séptimo elemento en abundancia en la corteza terrestre (aproximadamente 2,5% en masa) y el tercer elemento más abundante disuelto en el agua del mar. No se oxida en presencia del aire seco, pero cuando hay humedad se corroe con facilidad. Se emplea primordialmente como elemento de aleación del aluminio.
Sus minerales más importantes son: carnalita (es el más empleado y se halla en forma de cloruro de magnesio, que se obtiene del agua del mar), dolomita y magnesita.
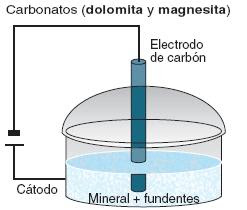
-Métodos de obtención:
Por un lado, podemos obtenerlo mediante la electrólisis. Este método lo usamos cuando lo obtenemos del agua del mar. Se aplica al cloruro de magnesio fundido, se coloca en una cuba que hace de cátodo y se introduce una barra de carbón que hace de ánodo. El magnesio liberado en estado de fusión, como es menos denso que el cloruro queda flotando, se retira por medio de la cuchara y se vierte en moldes.

Por otro lado, encontramos el método por reducción térmica
-Aplicaciones:
Tiene distintos usos como en lámparas relámpago y en pirotecnia por su combustión casi explosiva. También se usa como reductor para obtener otros metales y se utilizan en la fabricación de bicicletas, automóviles y motocicletas de competición. Se le da algunos usos en la aeronáutica.
5.2.-Berilio:

-Características:
Es
un metal que presenta una gran dureza, es ligero, tiene una alta
conductividad térmica y eléctrica y es resistente a la
corrosión. Es transparente a las radiaciones
electromagnéticas. Su brillo normalmente es vítreo y a
veces resinoso. Su dureza, de 7.5 a 8 y su densidad es de 2,7 g/cm3.
-Métodos de obtención:
Podemos obtenerlo mediante la reducción térmica de la dolomita calcinada o del óxido o mediante la reducción electrolítica, usando mezcla de haluros en estado fundido.
-Aplicaciones:
El berilio se usa en las ventanas de radiación para los tubos de rayos X por su baja absorción de rayos-X.
Se utiliza en las tuberías de muchos experimentos de alta energía de colisión de partículas. La rigidez del metal permite crear un vacío de gran alcance.
Es útil como componente de peso ligero de equipo militar y en la industria aeroespacial.
Es útil en herramientas que no produzcan chispas y los contactos eléctricos.
Son muy útiles las herramientas de berilio en minas navales o cerca de ellas. El berilio es un material no magnético y la mayoría de las minas navales detonan cuando entran en contacto con algo magnético.
Los espejos de berilio pueden usarse también en telescopios.
6.-Impacto Medioambiental
La evaluación y valoración del impacto ambiental producido por la extracción, transformación, fabricación y reciclado de productos no ferrosos constituye una técnica generalizada en todos los países industrializados y especialmente en la Unión Europea.
a) Durante la extracción de los minerales. Si esta extracción se realiza a cielo abierto, el impacto todavía puede ser mayor, ya que puede afectar a determinados hábitats.

b) Durante
la obtención de los distintos metales. Tenemos diversos tipos
de impactos:

1.Emisiones
- De
metales pesados (óxidos metálicos y vapores metálicos
volátiles),que son cancerígenos.
Gases, polvo e
hidrógeno gaseoso, que es muy corrosivo (peligroso para la
salud y el medio ambiente).
- Evitar que salgan de la fábrica, seleccionar emplazamiento y usar mascarillas.
2.Aguas residuales
- Aguas
de lavado y decapado de metales (soluciones alcalinas y ácidas)
y fangos.
- Neutralizar mediante productos químicos y vertederos controlados (evitar que haya escapes y puedan contaminar aguas subterráneas).

3.Contaminación acústica
.
- Causada por instalaciones y aparatos.
- Aislamiento
exterior. Si el nivel es superior a 80 decibelios, usar protectores
auditivos.
c) Durante el proceso de reciclado. El impacto ambiental es mucho menor, pero también importante.
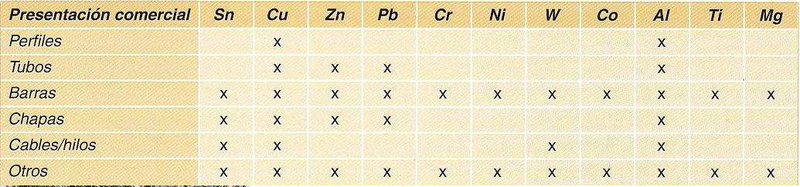
7.-Presentaciones Comerciales
Desde el punto de vista industrial, las presentaciones comerciales más usuales son:
TECNOLOGÍA
INDUSTRIAL METALES NO FERROSOS
CURSO 2015-16
1º BACHILLERATO DEPARTAMENTO DE FÍSICA Y QUÍMICA PRÁCTICA
1º BACHILLERATO (CIENCIAS) MATEMÁTICAS I CONTENIDOS PRIMERA PARTE
1º BACHILLERATO MATEMÁTICAS I TEMAS 3 TRIGONOMETRÍA NOMBRE 1
Tags: bachillerato metales, ferrosos, bachillerato, introducción, metales
- LESSON ELEMENT UNIT 2 LABORATORY TECHNIQUES LO3
- MEMORANDUM OF UNDERSTANDING BETWEEN WARSAW UNIVERSITY OF TECHNOLOGY WARSAW
- CAPITAL FEDERAL CIUDAD DE BUENOS AIRES 2444950328 2296283693
- PROGRAMA DE BECAS PARA CURSO DE VERANO DE ESTUDIOS
- ANEXA NR 56 ÎNTOCMIREA FIȘEI DE VERIFICARE A ÎNDEPLINIRII
- MODELLO D – DICHIARAZIONE SERVIZI SCUOLA INFANZIA PER GRADUATORIA
- THE SUMMARY CAUSE INFORMATION AND PROCEDURAL GUIDE PERSONAL INJURY
- F AG KROPPSØVING SKOLEÅRET 201516 KLASSETRINN 6KLASSE LÆRER ALEKSANDER
- M INISTERIO DE SALUD VICE MINISTERIO DE POLÍTICAS SECTORIALES
- C) POMOČ NA DOMU 1) KDO V OBČINI IZVAJA
- F BLANKO 1 ORMULIR PENDAFTARAN KETUASEKRETARIS PROGRAM STUDI DI
- BAB I PENDAHULUAN A DEFINISI REGISTRASI MAHASISWA ADALAH PROSES
- CLASSIFICATION BIOLOGICAL SCIENCE SYSTEMS BIOLOGY DIGITAL RNA SEQUENCING MINIMIZES
- PROJEKT USTAWA Z DNIA ………… 2014 R O ZMIANIE
- RATKO OROZOVIĆ BIOGRAFSKI PODACI I DRUŠTVENA AKTIVNOST RATKO OROZOVIĆ
- L PÉRIODE N°3 PS E LANGAGE AU
- EXPOSICIÓN DE MOTIVOS EL PRESENTE PROYECTO DE LEY MODIFICA
- 27 LA ADMINISTRACIÓN ACTUAL REQUIERE INSTRUMENTOS ESPECÍFICOS DE CONTROL
- WZÓR TA 06 (WERSJA KIEDY NFOŚIGW ZAWIERA UMOWĘ
- PROIECTUL „DEZVOLTAREA UTILIZĂRII DE INSTRUMENTE ELECTRONICE DE GESTIONARE A
- CHAPTER 2 – PROPERTIES OF MATERIALS STRESS IN MATERIALS
- SCHOOL NUTRITION PROGRAMS PROCUREMENT PROCEDURES AND CODE OF CONDUCT
- CENTAR ZA SOCIJALNU SKRB HRVATSKA KOSTAJNICA HRVATSKA KOSTAJNICA
- EGEEUSER FORUMOGF25 & OGFEUROPES SECOND INTERNATIONAL EVENT 26 MARCH
- PROTOKOLL 4 DATUM 20090421 NÄRVARANDE ORDFÖRANDE FREDRIK GÖTZMANN
- PROGRAMMA SOCI APRILEGIUGNO 2019 DATA ORA VISITE APPUNTAMENTO COSTO
- DATA SUBMISSION FOR ATCSECTORS FOR AIRAC UPDATES ADDRESSEES EUROCONTROL
- INSTITUTO DE NIVEL TERCIARIO “SAN FERNANDO REY” PROFESORADO EN
- BREVES REFLEXIONES SOBRE EL OBJETO DE ESTUDIO Y LA
- PLIEGO DE CONDICIONES PARA ADQUISICIÓN DE COMBUSTIBLES Y LUBRICANTES
ÐÏÀ¡±ÁÞŸ ¢ ¥ ÞŸŸŸX8C X8D X8E X8F X90 X91
 OFICINA DE REPRESENTACIÓN EN NAYARIT SUBDELEGACION ADMINISTRATIVA BASES PARA
OFICINA DE REPRESENTACIÓN EN NAYARIT SUBDELEGACION ADMINISTRATIVA BASES PARAWZÓR SPRAWOZDANIA SPORZĄDZANEGO PRZEZ PODMIOT ODBIERAJĄCY ODPADY KOMUNALNE OD
 UNIT OUTLINE AND PRESENTATION DATA OBJECTIVES AND INSTRUCTIONAL CUES
UNIT OUTLINE AND PRESENTATION DATA OBJECTIVES AND INSTRUCTIONAL CUESINTRODUCCIÓN Y EXPLICACIÓN DE LOS TIPOS DE INSIGNIAS EXISTEN
 Preguntas de Selección Múltiple con Única Respuesta (tipo 1)
Preguntas de Selección Múltiple con Única Respuesta (tipo 1)NEVERENDVIDA INFINITA GREEDISGOOD 999999 ORO Y MADERA AL TOKE
 PROVINCIA DE BUENOS AIRES DIRECCIÓN GENERAL DE CULTURA
PROVINCIA DE BUENOS AIRES DIRECCIÓN GENERAL DE CULTURAPROBLEM SET 5 FOR EACH OF THE FOLLOWING CONDUCT
 L ECTURA PENSAMIENTO POLÍTICO DE LA ILUSTRACIÓN VOLTAIRE (1694
L ECTURA PENSAMIENTO POLÍTICO DE LA ILUSTRACIÓN VOLTAIRE (1694 AMÉRICA MÓVIL EN AMÉRICA LATINA POR VENETA ANDONOVA (UNIVERSIDAD
AMÉRICA MÓVIL EN AMÉRICA LATINA POR VENETA ANDONOVA (UNIVERSIDAD Formato Auto que Ordena Pago al Auxiliar de Justicia
Formato Auto que Ordena Pago al Auxiliar de Justicia ENS LENGUAS VIVAS SOFÍA E BROQUEN DE SPANGENBERG NIVEL
ENS LENGUAS VIVAS SOFÍA E BROQUEN DE SPANGENBERG NIVELSAYIN ……………………… TARİH 2013 6331 SAYILI İŞ SAĞLIĞI
SMLOUVA O ZAJIŠŤOVÁNĹ PŘEPRAV VE VNITROSTÁTNÍ A MEZINÁRODNĹ SILNIČNĹ
 BECAS ESTIMULO 2013 BASES DOCUMENTOS DE REFERENCIA REGLAMENTO
BECAS ESTIMULO 2013 BASES DOCUMENTOS DE REFERENCIA REGLAMENTODERSIN KODU OTO203 DERSIN ADI GÜÇ AKTARMA ORGANLARI ULUSAL
 NA TEMELJU ČLANKA 10 ZAKONA O OTPISU DUGOVA FIZIČKIM
NA TEMELJU ČLANKA 10 ZAKONA O OTPISU DUGOVA FIZIČKIMZALBA MULTIVARIJANTNA STATISTIKA MZ M 59 A1S TIJANA ILIC
ROSA DEULOFEU PARE NOSTRE CALDES DE MONTBUI 1995 INTRODUCCIÓ