CÁLCULOS CON CONSTANTES DE EQUILIBRIO LA CONSTANTE DE EQUILIBRIO
Cálculos con constantes de equilibrio
Cálculos con constantes de equilibrio.
La constante de equilibrio (Kc) se calcula
sabiendo las concentraciones conocidas en el equilibrio. Una vez que
sepamos el valor de la constante de equilibrio, se puede utilizar
esta ecuación para resolver concentraciones de equilibrio
conocidas.
Ejemplo
del cálculo de la constante de equilibrio (Kc) :
S
 e
da el siguiente equilibrio a 230ºC
e
da el siguiente equilibrio a 230ºC
2NO(g) +
O2(g)
2NO2
Necesitamos saber las concentraciones para poder realizar la ecuación:
Concentraciones: [NO] = 0´0542M
[O2]
= 0´127 M
[NO2]
= 15´5M
*Resolución:
Reactivos Productos
K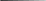

 c
= [NO2]2
2NO(g) + O2(g)
2NO2
c
= [NO2]2
2NO(g) + O2(g)
2NO2
[NO]2
· [O2]
Nota: Los cuadrados de la ecuación corresponden con el numero que vaya delante de cada fórmula. Para calcular la ecuación se sitúan los productos arriba dividido por los reactivos.
K c
= (15´5) 2
= 6´44 · 105 (
El resultado se da sin unidades)
c
= (15´5) 2
= 6´44 · 105 (
El resultado se da sin unidades)
(0´0542)
2 · (0´127)
Kc solo será constante si no hay cambio de
temperatura.
Usos
de la constante de equilibrio:
Ayudar a predecir la dirección de una mezcla para lograr el
equilibrio
- Calcular las concentraciones de reactivos y
productos una vez alcanzado el equilibrio.
Predecir la dirección de una reacción:
E j:
La constante de equilibrio para la
siguiente reacción es Kc = 54´3 a 430ºC
j:
La constante de equilibrio para la
siguiente reacción es Kc = 54´3 a 430ºC
H2(g)
+ I2(g)
2HI(g)

En el experimento se colocan 0´243 moles de H2, 0´146 moles de I2 y 1´98 moles de HI en un recipiente de 1L a 430ºC.
¿ Se llevará a cabo una reacción
neta que forme mas H2
e I2
, o bien mas HI?
- Se
sustituyen las concentraciones iniciales en la expresión de
equilibrio


 [HI]20
= (1´98)2
111
Cociente de reacción (Qc)
[HI]20
= (1´98)2
111
Cociente de reacción (Qc)
[H2]0 · [I2]0 (0´243)·(0´146)
El subíndice “0” se refiere a las concentraciones iniciales.
C omo
el cociente [HI]20
es mayor que Kc, este
sistema no esta en equilibrio.
omo
el cociente [HI]20
es mayor que Kc, este
sistema no esta en equilibrio.
[H2]0 · [I2]0
E l
HI reaccionará para formar H2
e I2,
disminuyendo el valor del cociente, por tanto la reacción
tendrá la dirección de derecha a izquierda H2(g)
+ I2(g)
2HI(g)
l
HI reaccionará para formar H2
e I2,
disminuyendo el valor del cociente, por tanto la reacción
tendrá la dirección de derecha a izquierda H2(g)
+ I2(g)
2HI(g)
El cociente de reacción (Qc) sirve para determinar que dirección tomará una reacción para estar en equilibrio, si se compara con la constante de equilibrio (Kc).
Hay 3 casos posibles:
Qc > Kc : La relación de las concentraciones iniciales de los productos entre los reactivos es demasiado grande. Para alcanzar el equilibrio, los productos se deben compartir en reactivos. El sistema avanzará de derecha a izquierda, consumiendo productos y formando reactivos, para alcanzar el equilibrio.
Qc = Kc : Las concentraciones iniciales son concentraciones en equilibrio.
Qc < Kc : La relación de concentraciones iniciales de productos a reactivos es muy pequeña. Para alcanzar el equilibrio los reactivos se convertirán en productos. El sistema va de izquierda a derecha, consumiendo reactivos y creando productos, para alcanzar el equilibrio.
Comparación entre Kc y Qc para una reacción :
A
 l
comenzar una reacción hay 0´249 moles de N2,
3´21 · 10-2
moles de H2
y 6´42 · 10-4 moles
de NH3 en
un reactor de 3´5 litros a 200ºC.
l
comenzar una reacción hay 0´249 moles de N2,
3´21 · 10-2
moles de H2
y 6´42 · 10-4 moles
de NH3 en
un reactor de 3´5 litros a 200ºC.
N2(g)
+ 3H2(g)
2NH3(g)
Si Kc vale 0´65 a esa temperatura ¿Estará el sistema en equilibrio?
Si no lo está, ¿ A que dirección se desplazará la reacción?
Resolución
Se calcula las concentraciones iniciales
[ N2]0
= 0´249 mol = 0´0711 M
N2]0
= 0´249 mol = 0´0711 M
3´5 L
[ H2]0
= 3´21 · 10-2
mol = 9´17 · 10-3
M
H2]0
= 3´21 · 10-2
mol = 9´17 · 10-3
M
3´5 L
[NH3]0 = 6´42 · 10-4 mol = 1´83 · 10-4
 3´5 L
3´5 L
2) Luego
calculamos Qc
[NH3]20 = [ 1´83 · 10-4]2 = 0´611 = Qc
[
 N2]0
· [H2]30
[ (0´0711) · (9´17 · 10-3)3]
N2]0
· [H2]30
[ (0´0711) · (9´17 · 10-3)3]
Como Qc es menor que Kc (0´65), el sistema no esta en equilibrio. El resultado sera un incremento del producto NH3 y disminuirán los reactivos H2 e I2 .
La reacción se efectúa de izquierda a derecha :
N 2(g)
+ 3H2(g)
2NH3(g)
2(g)
+ 3H2(g)
2NH3(g)
Bibliografía
Raymond Chang (1997). “Química”. Ed. Mc Graw Hill
Miguel Ángel Giménez Miralles
Tags: equilibrio (kc), el equilibrio, equilibrio, constantes, cálculos, constante
- ANSØGNINGSSKEMA TIL ANSØGNINGSPULJEN DRIFTSSTØTTE TIL LANDSDÆKKENDE FORENINGER FOR EN
- CONVENZIONE DI TIROCINIO FORMATIVO REGIONALE (ART 18 LEGGE REGIONALE
- 3 CONTINUING THE JOURNEY TRANSITION TIPS FOR PARENTS OF
- 2 DE LA MUERTE NATURAL LEWIS THOMAS1 EXISTE TAL
- TRECEREA DE LA ÎNVĂŢĂMÎNTUL PRIMAR LA CEL GIMNAZIAL CREŞTEREA
- GENERALITAT VALENCIANA HOSTING INSTITUTION OF THE BRANCH OFFICE FOR
- GUIDANCE NOTES FOR STREET COLLECTIONS THE CONDUCT OF STREET
- FACULTAD DE MEDICINA HUMANA ESCUELA PROFESIONAL DE MEDICINA HUMANA
- FECHA DEL CVA 06072020 PARTE A DATOS PERSONALES NOMBRE
- SUBMISSION FROM PATMALAR AMBIKAPATHY CO POBOX 7485 ST KILDA
- UNIVERSIDAD DE MURCIA INSTITUTO DE CIENCIAS DE LA EDUCACIÓN
- MINISTERIO DE SALUD SUBSECRETARÍA DE SALUD PÚBLICA FIJA CONFORMACIÓN
- „WYKORZYSTANIE METODY DOBREGO STARTU MARTY BOGDANOWICZ NA ZAJĘCIACH REWALIDACJI
- CURRICULUM VITAE PERSONAL DATA NAME SAMRAD MEHRABI
- SEMINARIO SOBRE CONSOLIDACIÓN CONTABLE Y FISCAL Y EL RÉGIMEN
- FORMULARIO DE SOLICITUD SALA DE USOS MÚLTIPLES DEL CONSEJO
- SOUTH CAROLINA GENERAL ASSEMBLY 116TH SESSION 20052006 S 644
- EXHIBIT LOG (EXLST) CLERK20 CASE NO CASE NAME CASE
- HODOGRAM AKTIVNOSTI VLADE NAZIV PROJEKTA SMANJENJE PLAĆA MILOM
- HASTA AYER DIANA WASSNER DE MALAMUD HASTA
- 5 EXPRESSION OF INTEREST (EOI) PROJECT NAME ASSIGNMENT I
- ANEXO Nº II ESPECIFICACIONES TÉCNICAS Nº ITEM DESCRIPCIÓN U
- TÉCNICAS DE INTELIGENCIA ARTIFICIAL INGENIERÍA ELECTRÓNICA PRÁCTICA 3 –
- AIDE AU STOCKAGE DE VIN CAS DES MODIFICATIONS
- THE 8TH TRAINING ON MAKING GOVERNANCE GENDER RESPONSIVE (THE
- DENETLEME RAPORU BALIKESİRMERKEZ AYŞEBACI 1ETAP TOPLU KONUTLARI TOPLU YAPI
- INEXISTENCIA DE VULNERACIÓN IMPROSPERIDAD DE LA TUTELA AL PRESENTARSE
- TOTAL ENERGY CONSUMPTION (EECCA CSI 26) ASSESSMENT
- R BITTE GRAU HINTERLEGTE FELDER AUSFÜLLEN! ESTAURANTBEWERTUNG FÜR KULINARISCHE
- VIRKSOMHETSPLAN ELVEBAKKEN MONTESSORIBARNEHAGE BA 2009 2012 ”HJELP MEG
 DECLARACIÓN RESPONSABLE MIEMBRO DEL EQUIPO DE TRABAJO NOMBRE Y
DECLARACIÓN RESPONSABLE MIEMBRO DEL EQUIPO DE TRABAJO NOMBRE Y CONVOCATORIA ENCUENTRO FECHA01022011 ANEXOINTERNO PÁGINA 5 DE 5 I
CONVOCATORIA ENCUENTRO FECHA01022011 ANEXOINTERNO PÁGINA 5 DE 5 I REPUBLIKA HRVATSKA ISTARSKA ŽUPANIJA OPĆINA FUNTANAFONTANE POVJERENSTVO ZA PROVEDBU
REPUBLIKA HRVATSKA ISTARSKA ŽUPANIJA OPĆINA FUNTANAFONTANE POVJERENSTVO ZA PROVEDBU DEPTH AND COMPLEXITY CHART TOPIC LANGUAGE OF THE DISCIPLINE
DEPTH AND COMPLEXITY CHART TOPIC LANGUAGE OF THE DISCIPLINE 3 S TYRELSEPROTOKOLL MÖTE 5 MÖTESDATUM MÖTESTID (BÖRJAN SLUT)
3 S TYRELSEPROTOKOLL MÖTE 5 MÖTESDATUM MÖTESTID (BÖRJAN SLUT) STREET NAMING & NUMBERING DATA INFORMATION TEL EMAIL
STREET NAMING & NUMBERING DATA INFORMATION TEL EMAIL EN COMMISSION OF THE EUROPEAN COMMUNITIES BRUSSELS XXX SEC(2007)
EN COMMISSION OF THE EUROPEAN COMMUNITIES BRUSSELS XXX SEC(2007)LESSON 12 THE CRUSADES SUGGESTED QUESTIONS THROUGHOUT ANGLOSAXON AND
HOWEVER IF IT YOUR SCANNER RELIES UPON OCR AS
 VII WORKSHOP DEL COMITÉ DE REGISTRO DE LA SOCIEDAD
VII WORKSHOP DEL COMITÉ DE REGISTRO DE LA SOCIEDAD Código Fga23 v01 Contenidos Programáticos Página 1 de 5
Código Fga23 v01 Contenidos Programáticos Página 1 de 5 S TATE OF CONNECTICUT JUDICIAL BRANCH INTERPRETER AND TRANSLATOR
S TATE OF CONNECTICUT JUDICIAL BRANCH INTERPRETER AND TRANSLATOR SOLICITUD DE CERTIFICADO DE PARTICIPACIÓN EN PROYECTOS DE INVESTIGACIÓN
SOLICITUD DE CERTIFICADO DE PARTICIPACIÓN EN PROYECTOS DE INVESTIGACIÓNA Informacje Ogólne Nazwa Pola Course Title Emotional Intelligence
 DECLARACIÓ RESPONSABLE PER A ESPORTISTES MAJORS D’EDAT ENNA AMB
DECLARACIÓ RESPONSABLE PER A ESPORTISTES MAJORS D’EDAT ENNA AMB BIODATA PEGAWAI GAMBAR A MAKLUMAT PERIBADI NAMA NO
BIODATA PEGAWAI GAMBAR A MAKLUMAT PERIBADI NAMA NO FUNDUSZ SPÓJNOŚCI PROJEKTY TRANSPORTOWE W POLSCE KOLEJE MODERNIZACJA LINII
FUNDUSZ SPÓJNOŚCI PROJEKTY TRANSPORTOWE W POLSCE KOLEJE MODERNIZACJA LINII REGLAMENTO TÉCNICO CENTROAMERICANO RTCA 67045008 NTON 03 080 –
REGLAMENTO TÉCNICO CENTROAMERICANO RTCA 67045008 NTON 03 080 –CEFA UTI IV ETIOPATOGENIA MICROBIOLOGICA PROGRAMA GENERAL BACTERIOLOGÍA
 ACUERDO DE COLABORACIÓN CON EL SERVICIO DE LOS
ACUERDO DE COLABORACIÓN CON EL SERVICIO DE LOS