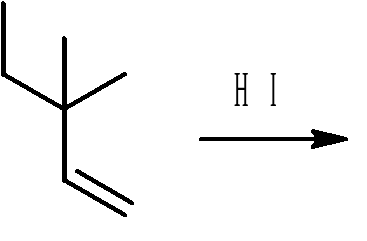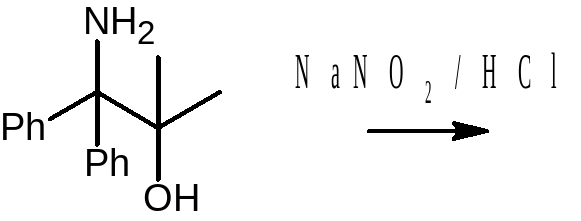ZADANIE 1 CHEMIA NIEORGANICZNA I ANALITYCZNA (AUTOR DR MARCIN
ZAŁĄCZNIK NR 1 NAZWA I ADRES WYKONAWCY ZADANIE0DPOWIEDZI NA ZAPYTANIA WYKONAWCÓW ZADANIE PN BUDOWA PRZYDOMOWYCH OCZYSZCZALNI
2002 GRUPA A ZADANIE 1 ZNALEŹĆ MACIERZ X TAKĄ
21 ZADANIE W ELEMENCIE R W CZASIE T1
3 WZÓR UMOWY NA ŚWIADCZENIA MEDYCZNE ZADANIE NR 3
4 SPECYFIKACJA PRZEDMIOTU DOFINANSOWANIA MODUŁ IOBSZAR CZADANIE NR
ZADANIE 1

Zadanie 1 Chemia nieorganiczna i analityczna (autor dr Marcin Strawski)
20,33
g pewnej soli X rozpuszczono w wodzie, a następnie
przeprowadzono jej elektrolizę. Na obu elektrodach wydzieliły
się gazy. Gaz wydzielony na anodzie w warunkach normalnych
zajmuje objętość 2,24 dm3.
Sam roztwór po elektrolizie zmętniał i zrobił
się galaretowaty. W celu analizy wyjściowej soli X
przeprowadzono także inne próby: po dodaniu roztworu
zawierającego jony chlorkowe lub siarczkowe, nie strącał
się żaden osad, za to biały osad pojawił się
po wprowadzeniu roztworu Na2CO3.
Inną naważkę soli, również
w ilości
20,33 g poddano analizie termicznej (DTA). W badanym zakresie
temperatur zaobserwowano cztery spadki masy. Dwa pierwsze przy
temperaturach 120 i 200C
były dwukrotnie większe od kolejnych przy temperaturach 240
i 340C.
Ubytek masy zmierzony w ostatnim etapie wyniósł 1,8 g, a
analiza masowa wydzielonego gazu charakteryzuje się dominującym
pikiem przy 18 m/z.
Podaj
pełny wzór soli, reakcje zachodzące w
elektrolizerze, jak i reakcje zachodzące
w czasie analizy
termicznej.
Zadanie 2 Chemia fizyczna (autor dr Marcin Strawski)
Obliczyć entalpię spalania 10,0 dm3 etynu (acetylen) odmierzonych w warunkach standardowych znając standardowe entalpie tworzenia:
etynu: ΔHtw = 226,51 kJ/mol
dwutlenku węgla: ΔHtw = -393.13 kJ/mol
wody: ΔHtw = -241.60 kJ/mol .
Zadanie 3 Chemia organiczna (autor dr Krzysztof Ziach)
Proszę zaproponować sposoby otrzymania z benzenu następujących bromopochodnych:

Komentarz i podpowiedzi do zadania:
Zadanie takie wcale nie jest proste i w wielu przypadkach wymaga przeprowadzenia bardzo wielu reakcji. Co więcej, zapewne nie ma tylko jednego poprawnego sposobu projektowania takich syntez, proszę do zadania podejść twórczo. Proszę się „nie bać” dużej liczby etapów, ale oczywiście, starać się by było ich jak najmniej.
Proszę wybierać takie reakcje które nie prowadzą „z definicji” do mieszaniny produktów, np. „złą” reakcją jest przedstawione poniżej nitrowanie fenolu, ponieważ produkty orto i para powstają w podobnych ilościach i są trudne do rozdzielenia:
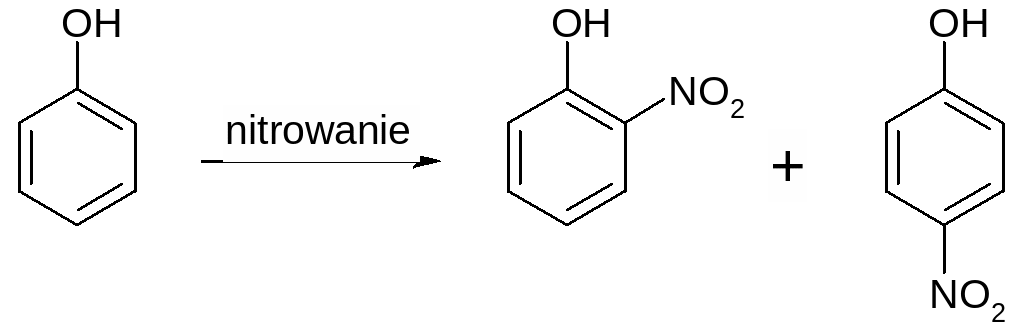
W związku z tym syntezy będą wymagały dodatkowych etapów i sprytnego stosowania grup ochronnych oraz sterowania wpływem kierującym podstawników).
„Trik 1” Wielokrotnie wykorzystuje się fakt, że bardzo łatwo można wprowadzić do cząsteczki grupę NO2 (która dezaktywuje pierścień i kieruje w położenie meta), wykonać konieczne etapy w jej obecności, a potem łatwo ją zredukować do grupy aminowej (która aktywuje pierścień i kieruje w położenie orto i para).
„Trik 2” Grupa aminowa jest bardzo użyteczna w takich syntezach i choć „nie ma jej” w finalnych związkach to często wprowadza się ją by:
zaktywować pierścień (tak by łatwo wprowadzić jakieś grupy w położenia orto i para względem grupy aminowej)
w
reakcji diazowania otrzymać diazopochodną, którą
bardzo łatwo przekształcić
w szereg innych grup
w reakcji Sandmayera
grupę aminową można (gdy przestaje być „potrzebna”) zamienić na atom wodoru, przekształcając ją w dizaopochodną, którą poddaje się reakcji z kwasem H3PO2.
„Trik 3”. Aktywację pierścienia, którą daje grupa aminowa, można obniżyć przekształcając ją w amid (zwykle acetamid). Co najważniejsze, taka grupa jest zawadą steryczną, niejako osłania pozycję orto i kieruje prawie wyłącznie w pozycję para. Jest to jeden z klasycznych sposobów rozwiązania problemu izomerów.
Wiedza szkolna zapewne nie pozwoli na otrzymanie wszystkich bromopochodnych. Jako dodatkowe źródła informacji polecamy akademickie podręczniki chemii organicznej McMurrego oraz Boyda i Morrisona.
Zadanie 4. Chemia organiczna (autor dr Karolina Pułka)
Proszę podać wszystkie oczekiwane produkty poniższych reakcji i przekształceń, w każdym przypadku uwzględniając możliwość przegrupowania produktów pośrednich lub substratów. Przegrupowanie zachodzi wtedy, gdy następuje reorganizacja wiązań i atomów.
Przegrupowanie karbokationów
Szereg trwałości karbokationów jest następujący:

O przegrupowaniu karbokationów mówimy wtedy, jeśli po migracji anionu wodorkowego lub prostej grupy alkilowej (np. -CH3) między sąsiadującymi atomami węgla, z mniej trwałego może powstać bardziej trwały karbokation.
|
a1) |
|
a2) |
|
a3) |
|
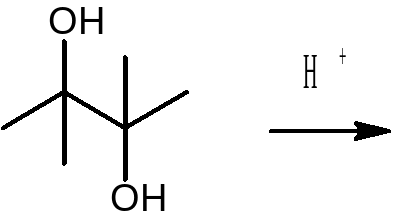
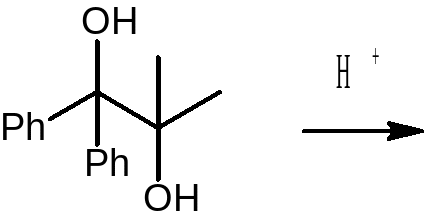
Przegrupowanie pinakolinowe
Diole
wicynalne w wyniku działania kwasów nieorganicznych
ulegają przekształceniu
w odpowiednie ketony.
Pierwszy etap tej reakcji polega na protonowaniu jednej z grup –OH,
następnie utraceniu cząsteczki wody z jednoczesnym wytworzeniem trwalszego karbokationu.
|
b1) |
|
b2) |
|
Deaminacja pinakolinowa
1,2-aminoalkohole ulegają reakcji przegrupowania do ketonów, pod wpływem działania NaNO2/HCl. W pierwszym etapie tworzą się sole diazoniowe (poznane w poprzednim zadaniu).
Alifatyczne jony diazoniowe są jednak bardzo nietrwałe.
|
c1) |
|
c2) |
|
Przegrupowanie Claisena
Etery
arylowo-allilowe oraz winylowo-allilowe w podwyższonej
temperaturze (> 250
C) ulegają przegrupowaniu Claisena do, odpowiednio,
podstawionych fenoli oraz aldehydów lub ketonów.
Zachodzi ono zgodnie z mechanizmem pericyklicznym, w którym
następuje jednoczesna reorganizacja elektronów, a stan
przejściowy ma postać pierścienia
6-członowego.
Poniżej przykład reakcji pericyklicznej:
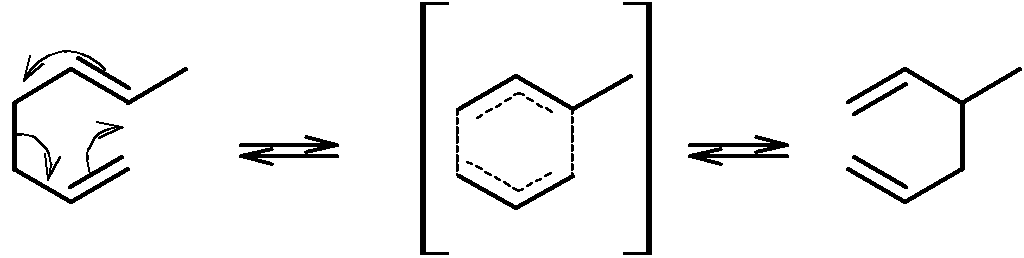
|
d1) |
|
d2) |
|
Zadanie 5
Wskaż
i popraw błędy w poniższych schematach reakcji (uwaga:
błędami nie są nieuwzględnienie stechiometrii ani
też brak szczegółowych warunków reakcji
np.
temperatury, rozpuszczalnika):
1)
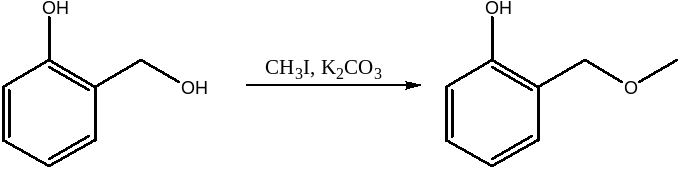
2)

3)

4)
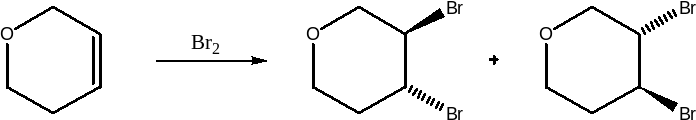
5)

6)
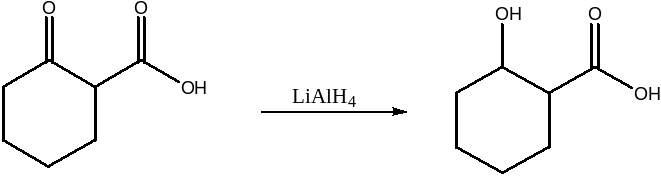
Zadanie 6
Zaproponuj metodę syntezy dla każdego związku z poniższych par izomerów:
1-bromopropanu i 2-bromopropanu z alkoholu izopropylowego,
m-chloroaniliny i p-chloroaniliny z benzenu,
N,N-dimetylobenzyloaminy i N,N-dimetylo-m-toluidyny z benzenu,
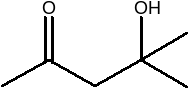 i
i
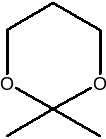 z dowolnych substratów,
z dowolnych substratów,
dipeptydów: Ala-Gly oraz Gly-Ala z aminokwasów.
Zadanie 7
Alkohol A o wzorze sumarycznym C4H10O poddano reakcji z kwasem siarkowym(VI), zaś na izomeryczny alkohol B podziałano kwasem bromowodorowym otrzymując nieizomeryczne produkty, odpowiednio C i D. W widmach 1H NMR związków A, B, C, D widoczna jest następująca ilość sygnałów: A – 2, B – 4, C – 2, D–3.
Podaj wzory i nazwy związków A, B, C, D.
Nazwij mechanizmy reakcji A C oraz BD.
Jaki będzie wynik reakcji A i B z ZnCl2/HCl (odczynnik Lucasa)?
A i/lub B ulega(ją) reakcji z K2Cr2O7 tworząc produkt(y) E i/lub F, w których widmie IR pojawia się charakterystyczne silne pasmo adsorpcji. Podaj budowę E i/lub F, przybliżoną liczbę falową pasma charakterystycznego oraz grupę odpowiedzialną za jego występowanie.
Wspieranie w rozwoju uczniów wybitnie uzdolnionych w zakresie nauk matematyczno-przyrodniczych.
Projekt współfinansowany z Europejskiego Funduszu Społecznego
w ramach Programu Operacyjnego Kapitał Ludzki
46 ROČNÍK FYZIKÁLNEJ OLYMPIÁDY ŠKOLSKÝ ROK 200405 ZADANIE
5 EKSTRAKCJA ZADANIE 1 W FAZIE WODNEJ O OBJĘTOŚCI
6 WSOWL POSTĘPOWANIE PRZEDSIĘBIORSTWA NA RYNKU DOSKONALE KONKURENCYJNYM ZADANIE
Tags: (autor dr, organiczna (autor, (autor, marcin, chemia, zadanie, analityczna, nieorganiczna
- S VEUČILIŠTE U ZADRU ELABORAT O STUDIJSKOM PROGRAMU OBRAZAC
- Karta Kompetencji Praktykanta i Stopień Praktyka Wstępna Imię i
- ALTERAÇÃO DE MODALIDADE O MUNICÍPIO QUE DESEJE ALTERAR A
- NÁZOV VYSOKEJ ŠKOLY NÁZOV FAKULTY PREŚOVSKÁ UNIVERZITA V PREŠOVE
- CCOF GLOBALGAP CERTIFICATION PROGRAM APPLICATION TO APPLY FOR CCOF’S
- ZAŁĄCZNIK NR 7 DATA ZŁOŻENIA SPRAWOZDANIA RAMOWY WZÓR
- CARACTERIZACION METABOLICA DE SUJETOS CON SOBRE PESOOBESIDAD APARENTEMENTE SANOS
- POLJA OZNAČENA SA SU OBAVEZNA POLJA ZAHTJEV KOJI
- LA DECONSTRUCCIÓN DE LA PINTURA DUVAN O LA INVENCIÓN
- ANDOAINGO UDALA LEITZARAN ABENTURA EGITASMOAN PARTE HARTZEKO BAIMENA EKINTZAREN
- BILL VON HIPPEL (UNSW) DENISE SEKAQUAPTEWA AND PENELOPE ESPINOZA
- LIETUVOS AKUŠERIŲGINEKOLOGŲ DRAUGIJOS ETIKOS KODEKSAS LIETUVOS AKUŠERIŲGINEKOLOGŲ DRAUGIJOS ETIKOS
- INSERT NAME OF FACULTY OR DIVISION HERE APPLICATION TO
- KONYA TİCARET ODASI DIŞ TICARET SERVISI TARIH
- MULTIDIMENSIONAL AND INTEGRATED PEACE OPERATIONS TRENDS AND CHALLENGES BEIJING
- Procedura P42301 Wydanie 5 z Dnia 15032012 r Nadzór
- OCTUBRE DE 2015 NORMATIVA E INFORMACIÓN DE INTERÉS PARA
- ETUDE PRESVAS SYNDROME D’ENCÉPHALOPATHIE POSTÉRIEURE RÉVERSIBLE (PRES) ASSOCIÉ AUX
- SREDNJA ŠKOLA ČAKOVEC JAKOVA GOTOVCA 2 40000 ČAKOVEC OIB
- KEMET FAQ A COMPILATION OF OFFICIAL FAQ AND QUESTIONS
- COUNTY OF PASSAIC BID TALLY SHEET SHERRY ARVANITAKIS QPA
- R4‑2 REQUIREMENTS AS TO SIZE FORM IDENTIFICATION AND FILING
- ANMÄLAN ENLIGT 6 KAP 6 § VAPENLAGEN (199667) TILL
- OBRAZAC ZA PROCJENU DODATNIH I POSEBNIH UVJETA NAZIV ZADRUGE
- CHÍNH PHỦ CỘNG HÒA XÃ HỘI CHỦ NGHĨA
- PLANTILLAS CIRCUITO SUB 20 (SEGUNDA CONCENTRACIÓN) REAL MADRID
- EGPGENETIQUE 20 RUE LEBLANC 75908 PARIS CEDEX 15 QUESTIONNAIRE
- 11 LA IMPLEMENTACIÓN DE CURSOS EN LÍNEA EN UNA
- WILLIAM L STULL PROFESSOR OF RHETORIC AT THE UNIVERSITY
- 1 DETERMINACION DE TIPOS DE EMBALAJE PARA MATERIALES 12
 CBD CONVENTION ON BIOLOGICAL DIVERSITY PRESS RELEASE FOR
CBD CONVENTION ON BIOLOGICAL DIVERSITY PRESS RELEASE FOR CDC UNIFIED PROCESS LESSONS LEARNED POST PROJECT SURVEY
CDC UNIFIED PROCESS LESSONS LEARNED POST PROJECT SURVEY  CALAHORRA GEOGRAFÍA 2º BTO TEMA 2 COMENTARIO DE UN
CALAHORRA GEOGRAFÍA 2º BTO TEMA 2 COMENTARIO DE UNBOLSA DE SECRETARIOS INTERVENTORES AÑO 2010 CONVOCATORIA ORDEN
COMMENTS FROM GRACE DAVIES CHANGES MADE TO SOUTH GLOUCESTERSHIRE’S
 PROYECTO ALACIMA ACTIVIDAD LOS MACRONUTRIENTES Y MICRONUTRIENTES EN EL
PROYECTO ALACIMA ACTIVIDAD LOS MACRONUTRIENTES Y MICRONUTRIENTES EN ELBODIL ENGELS ERINDRINGER OM TJENESTEGØRING PÅ ALLINGÅBRO STATION GLIMT
EMPLOYMENT OF WASTE SAND TO COMPOSE FIBRE REINFORCED CEMENT
2 AKTI VLADE PROPISIVANJEM KRITERIJUMA ZA UTVRĐIVANJE USLOVA
DESDE INIA LB EJEMPLOS DE INNOVACIÓN UN EJEMPLO PARA
FIRST TEST OF NATIVE INTERPRETER SUPPOSING THAT DMP RESIDES
LITURGIA DE DIFUNTOS LA MUERTE ORIGINA INFINIDAD DE SENTIMIENTOS
 METHANE VS PROPANE AS A FUEL SOURCE C11209 TEACHER
METHANE VS PROPANE AS A FUEL SOURCE C11209 TEACHER CPUSH (UNIT 1 4) NAME BRITISH COLONIZATION IN
CPUSH (UNIT 1 4) NAME BRITISH COLONIZATION INEVOLUTION OF ABSOLUTISM IN FRANCE HENRY OF NAVARRE BECOMES
LAND TITLE ACT FORM 31 (SECTION 215 (1)) NATURE
 AKADEMICKI INKUBATOR PRZEDSIĘBIORCZOŚCI (AIP) – KONCEPCJA CELE
AKADEMICKI INKUBATOR PRZEDSIĘBIORCZOŚCI (AIP) – KONCEPCJA CELE FREQUENTLY ASKED QUESTIONS ON REQUIRED RECEIPTS REFERENCES A) JOINT
ABSTRAKT TENKNING DISSE SPØRSMÅL TESTER EVNEN TIL ABSTRAKT TENKNING
TOEPASSING VAN HET VERLAAGD BTWTARIEF VAN 6 OP ONROERENDE